Zeolit

- Posted by admin
- Posted in Artikel, Publikasi Ilmiah
Bagaimana Zeolit Alam Klinoptilolite dapat Berperan dalam Pembuatan Biodiesel dari Minyak Nabati?
Biodiesel adalah bahan bakar terbarukan yang dibuat dari bahan baku lemak hewani maupun nabati berupa metil ester asam lemak yang telah lama disebut sebagai pengganti minyak bumi. Sifat kimia biodiesel yang dihasilkan sangat bergantung dari asal bahan bakunya. Komposisi kimia dari beberapa bahan baku biodiesel tercantum dalam table berikut (nilai dalam persentase).

Sumber: Organic Chemistry, W.W.Linstromberg, D.C.Heath and Co.,Lexington, MA, 1970
Pembuatan biodiesel pertama kali dilakukan oleh E.Duffy dan J. Patrick pada tahun 1853, sebelum mesin diesel pertama kali ditemukan. Baru setelah empat puluh tahun kemudian, seorang ilmuwan Rudolf Diesel berhasil merakit mesin diesel pertama pada tahun 1893 di Augsburg, Jerman yang kemudian diperkenalkan di World’s Fair di Prancis. Pada waktu itu, biodesel yang digunakan berasal dari minyak kacang tanah.
Seiring dengan perkembangan pembuatan biodiesel saat ini, bahan baku dari lemak nabati lebih dominan dan sudah mencapai skala industri. Minyak kelapa sawit merupakan salah satu bahan baku biodiesel yang cukup produktif. Satu hektar tanaman kelapa sawit mampu menghasilkan 3,5 ton minyak nabati, hal ini lebih banyak dibandingkan dengan tanaman kanola yang hanya mampu menghasilkan 0,8 ton minyak nabati per hektar nya.
Biodiesel diproduksi dengan cara mereaksikan lemak (triglyceride) dengan alkohol dalam proses yang disebut transesterifikasi. Reaksi tersebut menghasilkan biodiesel dan gliserol sebagai produk sampingan.
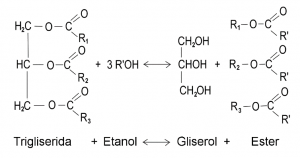
(1)
(2)
Untuk mempercepat reaksi dan menggeser keseimbangan ke kanan, maka variable yang berpengaruh perlu dikendalikan dan dipilih nilainya agar diperoleh hasil yang sebaik-baiknya. Variabel yang perlu dikendalikan meliputi: waktu, konsentrasi, pencampuran, perbandingan pereaksi, katalisator, suhu, dan penghilangan salah satu hasil (Kirk Othmer, 1992).
Waktu
Pada tahap awal, reaksi ke kiri hanya sedikit, sehingga dianggap reaksi hanya berlangsung ke kanan. Semakin lama waktu reaksi, semakin banyak hasil yang diperoleh, karena kesempatan zat-zat pereaksi untuk saling bertumbukan semakin besar. Kejadian ini hanya akan berlangsung sampai waktu tertentu, terdapat waktu optimal yang diperlukan untuk masing-masing proses.
Konsentrasi
Kecepatan reaksi sebanding dengan konsentrasi zat-zat pereaksi. Oleh karena itu, agar reaksi berjalan cepat diperlukan zat pereaksi dengan kemurnian tinggi. Adanya air dan zat pengotor di dalam zat pereaksi akan menurunkan hasil.
Pencampuran
Pencampuran yang baik akan memperlancar jalannya reaksi. Salah satu cara pencampuran dapat dilakukan dengan pengadukan, yang akan memperbesar turbulensi, sehingga meningkatkan tumbukan antara molekul-molekul zat pereaksi. Cara pencampuran tergantung dari jenis reactor yang digunakan. Pada reactor batch, pencampuran dapat dilakukan dengan pengaduk merkuri atau pengaduk magnet. Pada reaktor jenis autoklaf , pencampuran dapat dilakukan dengan memutar autoklaf. Pada reactor kolom berpulsa, pencampiran zat-zat pereaksi dengan menggerakkan naik turun lempeng-lempeng yang ada.
Perbandingan Pereaksi
Pemakaian salah satu pereaksi melebihi perbandingan stoikiometri, memperbesar kemungkinan terjadinya tumbukan, sehingga konstanta kecepatan reaksi juga akan bertambah.
Suhu
Menurut persamaan Arrhenius, semakin tinggi suhu maka reaksi akan berjalan semakin cepat. Namun hal ini tidak berlaku secara linier, ada batas tertentu suhu harus dijaga agar tidak terlalu tinggi.
Penghilangan salah satu hasil
Sesuai dengan persamaan (1) di atas, gliserol adalah hasil samping pada reaksi transesterifikasi pembuatan biodiesel. Apabila setiap gliserol yang terbentuk, kemudian diikat maka reaksi ke kiri akan kecil sekali sehingga keseimbangan akan cenderung bergeser ke kanan.
Katalisator
Penambahan katalisator mengaktifkan zat-zat pereaksi, sehingga tumbukan yang terjadi semakin banyak, dan reaksi berlangsung semakin cepat.
Dalam produksi biodiesel pada umumnya menggunakan katalisator homogen seperti NaOH dan KOH, meskipun katalisator heterogen dan enzim juga dapat digunakan. Katalisator homogen memiliki kelemahan yaitu proses pemisahannya dari biodiesel yang realtif kompleks sehingga akan meningkatkan biaya produksi. Di samping itu, katalis homogen seperti NaOH yang sering digunakan sangat higroskopis sehingga menyulitkan dalam penanganannya. Untuk mengatasi hal tersebut, dapat digunakan alternative katalisator heterogen seperti kalsium karbonat dan zeolite. Penggunaan katalisator heterogen ini dapat menurunkan harga produksi, proses pemisahannya sangat mudah sehingga hasil ester dan gliserol yang diperoleh memiliki kualitas tinggi.
Zeolit merupakan mineral yang terdiri dari kristal alumino silikat terhidrasi yang mengandung kation alkali atau alkali tanah. Struktur zeolit berupa kristal polimer anorganik dengan kerangka tetrahedral AlO4 dan SiO4 . Rumus struktur zeolit dapat dituliskan sebagai Mx/n [ (AlO2)x .(SiO2)y .wH2O], dengan n adalah valensi dari kation M, w adalah jumlah molekul air per unit sel, x dan y adalah total jumlah tetrahedral per unit sel (Haslego, 1999).
Katalis yang sering digunakan dalam alkoholisis minyak nabati adalah natrium hidroksida , dengan menyisipkan logam natrium pada zeolit akan memberikan sifat katalitik yang sesuai sehingga dapat meningkatkan kecepatan reaksi alkoholisis .
Minyak nabati merupakan trigliserida dengan gugus karbonil mendominasi karakter kimianya. Oksigen pada gugus karbonil memiliki dua pasang elektron bebas sehingga oksigen akan bersifat nukleofilik dan cenderung menarik kation untuk mencapai keseimbangan yang optimum. Pada gugus karbonil inilah terjadi proses penyerangan trigliserida oleh alkohol dengan bantuan katalisator zeolit.
Pada struktur zeolit, semua atom Al dalam bentuk tetrahedral sehingga atom Al akan bermuatan negatif karena berkoordinasi dengan atom oksigen. Zeolit dapat dimanipulasi dengan menyisipkan logam tertentu sehingga memiliki sifat katalitik tertentu (Haslego, 1999). Zeolit alam yang diaktifkan dengan NaOH akan bersifat basa dan mengikat ion Na+, sehingga sering disebut Na-zeolit ( O – Na+ ).


Mekanisme reaksi yang terjadi di dalam reaksi alkoholisis minyak jarak dengan katalisator Na-zeolit, adalah sebagai berikut:
- Pengaktifan alkohol oleh zeolit
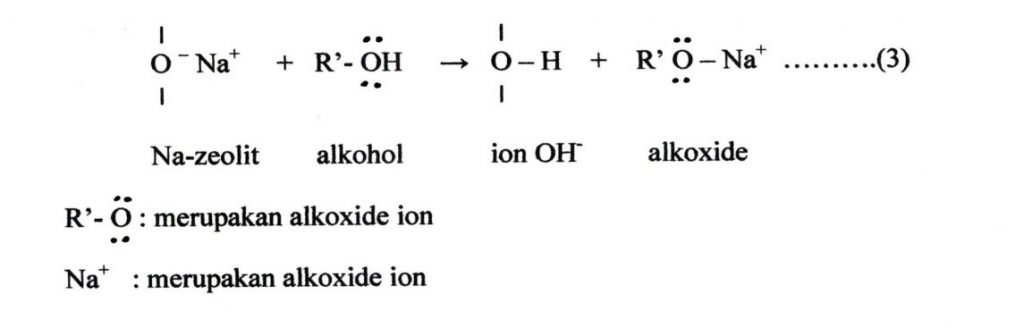
Na-zeolit akan mengaktifkan alkohol membentuk alkoxide. Alkohol mendifusi ke permukaan luar katalis, sehingga terjadi pertukaran ion H+ dengan ion Na+ .
- Pengaktifan trigliserid oleh zeolit
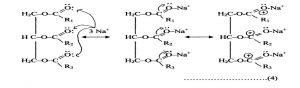
Minyak mendifusi ke permukaan luar katalis, sehingga ion Na+ pada zeolit akan mendekati gugus karbonil. Na+ akan mencari posisi paling nukleofilik, sehingga Na+ akan mendekati O yang mempunyai dua pasang elektron bebas. Oksigen memberikan satu pasang elektronnya untuk dipakai bersama-sama dengan Na+ sehingga oksigen menjadi kekurangan elektron. Karena oksigen bersifat elektronegatif, maka O akan berusaha menarik pasangan elektron pada ikatan rangkap C. Oleh karena atom C telah memberikan sebagian elektronnya untuk dipakai bersama O, maka C pada ikatan rangkap menjadi bermuatan positif (disebut carbocation atau C+).
- Pembentukan Ester
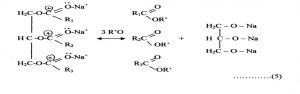
Pada saat pencampuran antara zeolit dengan minyak dan alkohol, akan terjadi pengaktifan minyak dan alkohol oleh ion Na+ . Kemudian alkohol yang teraktifkan akan bereaksi dengan minyak yang sudah teraktifkan. Alkoxide memiliki ion R’- O – yang merupakan alkoxide ion dengan dua pasang elektronnya, sedangkan trigliserid yang teraktifkan mempunyai atom C yang bermuatan positif, sehingga R’- O– cenderung mendekati atom C untuk memberikan satu pasang elektronnya untuk dipakai bersama-sama. Setelah terjadi pengaturan elektron untuk mencapai kesetimbangan muatan (sesuai aturan oktet) maka terbentuk ester.
- Pelepasan Na-zeolit

Pada pembentukan alkoxide, terbentuk juga ion OH–, ion ini akan bertukar tempat dengan ion Na+ sehingga terbentuk gliserol. Zeolit dalam bentuk O-Na+ akan terlepas lagi.
Zeolit yang akan digunakan sebagai katalisator, sebelumnya diaktifkan dengan NaOH sehingga mengikat ion Na+. Hal ini menyebabkan semakin banyak katalisator yang digunakan, semakin banyak pula ion Na+ yang ditambahkan kedalam larutan, sehingga proton yang dimiliki alkoxide juga semakin banyak. Banyaknya proton yang dimiliki menyebabkan alkoxide semakin asam (menurut Bronsted), sehingga penyerangan gugus karbonil menjadi semakin cepat dan konversi gliserid yang dihasilkan juga semakin besar.
Pemanfaatan zeolit alam sebagai katalisator dalam reaksi pembuatan biodiesel akan menambah nilai guna bahan tersebut, yang juga merupakan kekayaan alam Indonesia.
(by RSH 2019)
Groggins, P.H., 1958, “Unit Process in Organic Synthesis”, 5.ed., pp. 710-715, McGraw-Hill Book Company, Inc., New York.
Haslego, C., 1999, “Green Chemistry with Zeolite Catalyst”, www.cheresources.com.
Kirk, R.E., and Othmer, D.F., 1979, “Encyclopedia of Chemical Thecnology” vol.5, pp.817-819, Interscience Encyclopedia, Inc., New York.
